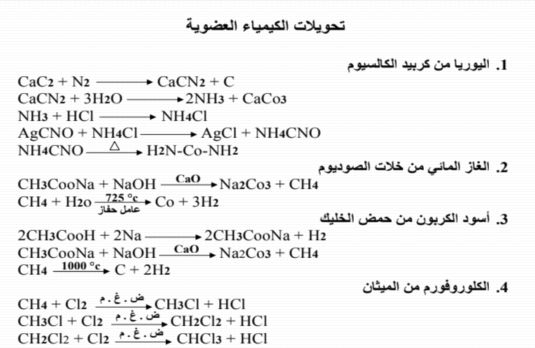
جميع افكار معادلات الكيمياء العضوية بالاجابات النموذجية...
بسم الله الرحمن الرحيم , يشتكي اغلب طلاب الثانوية العامة من مادة الكيمياء وتحديدا الكيمياء العضوية وبالاخص سؤال كيف تحصل علي مركب من مركب آخر
في طلاب كانت بتسأل عن كيفية حفظ معادلات الكيمياء العضوية .
-------------
اذا كنت تريد ان تحصل علي الدرجة النهائية لا تحاول ان تحفظ المعادلات بالرموز فقط بل حاول فهمها وتسميعها باسم العنصر وليس رمزه .
-----
طيب ازاي أفهم المعادلة
هقولك كام عنوان واشرحلك التفاصيل بعدين
أولا كل معادلة ليها حكاية، قصة، لازم تعرف القصة دي إيه
يعني لو قلنا مثلا العضوية
تفاعل الإيثانول مع حمض الكبريتيك المركز مثلا
ده له قصة بسيطة أوي
حمض الكبريتيك المركز ده ( مية النار لو تسمع عنها ) من اسمها كدة مية نار، بتحرق ليه؟ عشان بتنتزع المياه من أي حاجة
عشان كدة بنضيفها في تفاعل الأسترة لمنع التفاعل العكسي ( تعليل جاي في الامتحان )
يعني لما نضيفها على الإيثانول هتاخد منه جزئ مياه وهيتبقى في الآخر إيثلين
C2H5OH ----H2SO4----> C2H4+H2O
بسيطة أوي
ثانيا في مركبات خصائصها معروفة، معرفتها هتسهل عليك أوي: خد عندك
حمض كبريتيك مركز ... نازع للماء
خليط من حمض النيتريك والكبريتيك المركز ... اسمه خليط النيترة وبيعمل نيترة يعني بيدخل للمركب مجموعة نيترو NO2
الهيدروجين .. يعمل هدرجة ويكسر الروابط الثنائية ويعمل مركب مشبع وهكذا
ثالثا في مركبات كتير أوي ليها تفاعل واحد في الكيمياء عندك، عشان متتلخبطش فيها تبقى عارف أنك لما تشوف المركب ده وانت مغمض يبقى التفاعل بتاعه هو كذا
مثلا
أول ما تشوف كربيد كالسيوم .. وانت مغمض تقول إضافة 2 جزئ ماء ( تفة مزدوجة ) ويطلع اسيتلين
أول ما تشوف أسيتات صوديوم يبقى تقول تقطير جاف ويطلع ميثان وانت مغمض
أول ما تشوف أوكتان
يبقى تكسير حراري حفزي وهكذا
المهم افهم المعادلة قبل ما تفكر تحفظها
تحميل : تحويلات الكيمياء العضوية والعناصر الانتقالية من هنااا
بسم الله الرحمن الرحيم , يشتكي اغلب طلاب الثانوية العامة من مادة الكيمياء وتحديدا الكيمياء العضوية وبالاخص سؤال كيف تحصل علي مركب من مركب آخر
في طلاب كانت بتسأل عن كيفية حفظ معادلات الكيمياء العضوية .
-------------
اذا كنت تريد ان تحصل علي الدرجة النهائية لا تحاول ان تحفظ المعادلات بالرموز فقط بل حاول فهمها وتسميعها باسم العنصر وليس رمزه .
-----
طيب ازاي أفهم المعادلة
هقولك كام عنوان واشرحلك التفاصيل بعدين
أولا كل معادلة ليها حكاية، قصة، لازم تعرف القصة دي إيه
يعني لو قلنا مثلا العضوية
تفاعل الإيثانول مع حمض الكبريتيك المركز مثلا
ده له قصة بسيطة أوي
حمض الكبريتيك المركز ده ( مية النار لو تسمع عنها ) من اسمها كدة مية نار، بتحرق ليه؟ عشان بتنتزع المياه من أي حاجة
عشان كدة بنضيفها في تفاعل الأسترة لمنع التفاعل العكسي ( تعليل جاي في الامتحان )
يعني لما نضيفها على الإيثانول هتاخد منه جزئ مياه وهيتبقى في الآخر إيثلين
C2H5OH ----H2SO4----> C2H4+H2O
بسيطة أوي
ثانيا في مركبات خصائصها معروفة، معرفتها هتسهل عليك أوي: خد عندك
حمض كبريتيك مركز ... نازع للماء
خليط من حمض النيتريك والكبريتيك المركز ... اسمه خليط النيترة وبيعمل نيترة يعني بيدخل للمركب مجموعة نيترو NO2
الهيدروجين .. يعمل هدرجة ويكسر الروابط الثنائية ويعمل مركب مشبع وهكذا
ثالثا في مركبات كتير أوي ليها تفاعل واحد في الكيمياء عندك، عشان متتلخبطش فيها تبقى عارف أنك لما تشوف المركب ده وانت مغمض يبقى التفاعل بتاعه هو كذا
مثلا
أول ما تشوف كربيد كالسيوم .. وانت مغمض تقول إضافة 2 جزئ ماء ( تفة مزدوجة ) ويطلع اسيتلين
أول ما تشوف أسيتات صوديوم يبقى تقول تقطير جاف ويطلع ميثان وانت مغمض
أول ما تشوف أوكتان
يبقى تكسير حراري حفزي وهكذا
المهم افهم المعادلة قبل ما تفكر تحفظها
تحميل : تحويلات الكيمياء العضوية والعناصر الانتقالية من هنااا












https://mega.nz/file/jjwCkYoC#hd9CbJoBVnbfO14i-SO44IhAJ0CVl1bSTQHZJqwevp4
Professorالثلاثاء 05 يناير 2021, 11:06 pm